|
Bio&Biotech
 >
Wechselwirkungen
>
Wechselwirkungen
WechselwirkungenIonische Protein-Polysaccharid-Interaktionen als Grundlage für Emulsionen mit besonderen EigenschaftenDieser Beitrag gibt einen Einblick in die „molekulare“ Emulsionsbildung, bei der Interaktionen zwischen ionischen Biopolymeren zur Erzeugung unterschiedlicher Mikro- und Makrostrukturen mit besonderen Eigenschaften führen. Bei der Herstellung von Öl-in-Wasser-Emulsionen ermöglichen derartige Interaktionen die Gestaltung unterschiedlicher Öl-Wasser-Grenzschichten und damit zugleich die Einstellung verschiedener Gebrauchseigenschaften. Obwohl Reaktionen zwischen Proteinen und Polysacchariden schon seit über 70 Jahren zur Einstellung bestimmter Eigenschaften (z.B. Konsistenzgebung, Emulsionsbildung) gezielt genutzt werden, eröffnen diese weiterhin viele neue Möglichkeiten zur Erzielung spezieller Emulsionseigenschaften. Das Interesse an der Reduzierung des Einsatzes synthetischer Emulgatoren und chemisch modifizierter Zusatzstoffe hat zur erhöhten Nachfrage nach natürlichen bzw. nur gering behandelten biologischen Rohstoffen als Rezepturbestandteil im Food-, Kosmetik- und Pharmabereich geführt. Der kombinierte Einsatz von ionischen Biopolymeren bzw. polymeren Polyelektrolyten (Proteine, Polysaccharide) erleichtert die Herstellung von „Naturstoff“-Emulsionen mit speziellen Verkapselungs- und Freisetzungs- sowie Viskositäts- und Konsistenzeigenschaften. Innovationspotenzial der Polyelektrolyt-Interaktionen Zu den vielfältigen Anwendungs- und Forschungsgebieten der Nutzung von Interaktionen zwischen polymeren Polyelektrolyten gehören u.a. die Medizin (Blutaustauscher, Gerinnungshemmer, Vermeidung der Proteinadsorption an Implantaten), die Pharmazie (Nanoverkapselung von Wirkstoffen, Immobilisierung von Enzymen und Mikroorganismen, Hydrogele mit kontrollierter Wirkstofffreisetzung, Träger für Wirkstoffe), die Chemie und Technik (Wasserbehandlung, ökologische Zusätze für schaumbildende Bohrspülungen, Kühlschmierstoffe mit Filmbildung und bestimmter Viskosität für die Metallbearbeitung, Membranen für die Alkohol-Wasser-Trennung, Konsistenzgebung von Baustoffgemischen). Bei der hier vorgestellten Emulsionsherstellung bestehen die genutzten Interaktionen in der milieuabhängigen Reaktion zwischen den Proteinen (z.B. Aminogruppen der Proteine; -NH3+) und den anionischen Polysacchariden (Carboxylgruppen -COO- oder Sulfogruppen -OSO3-, z.B. -COO-···+3HN-). Während die Proteine aufgrund ihres amphoteren Charakters unterhalb des isoelektrischen Punktes (IEP) positiv geladen sind, weisen diese oberhalb des IEP – wie die Polysaccharide – eine negative Ladung auf (Abb. 1). Im pH-Bereich um 4 und 5 befindet sich bei vielen Proteinen der IEP mit der geringsten Ladung. Über die Veränderung der Ladungszustände (repulsiv oder attraktiv) und der Gesamtladung ermöglichen die elektrostatischen Wechselwirkungen die Bildung von Protein-Polysaccharid-Komplexen (löslich oder unlöslich), die als Emulgatoren und Stabilisatoren für disperse Systeme eingesetzt werden können [1]. Weiterhin sind hierüber die Einzeltropfenverteilung, Tropfenaggregation, Phasenstabilität, Koaleszenzstabilität, rheologische Eigenschaft und Konsistenz einstellbar. Dies bestimmt Einsatzgebiete und Gebrauchseigenschaften der Emulsionen. Im Mittelpunkt der Forschung steht z.Z. die Nutzung der Wechselwirkungen von Milch- und Pflanzenproteinen mit verschiedenen ionischen Polysacchariden (u.a. modifizierte Pektine, Na-Carboxymethylcellulose, Carrageen, Xanthan, Dextransulfat, Gummi arabicum [1]). Über elektrostatische Wechselwirkungen (pH-Wert-abhängig) und Auswahl der ionischen Biopolymere ermöglichen die Protein-Polysaccharid-Interaktionen die Bildung neuartiger Emulsionssysteme, geeignet zum Einschluss unterschiedlichster Komponenten (Vitamine, Wirkstoffe, Aromen, mehrfach ungesättigte Fettsäuren, Enzyme u.a.m.) sowie zur Einstellung der Stofffreisetzung.
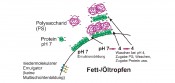
Abb.1 Bereiche des Ladungspotenzials von Proteinen (Beispiel für β-Lactoglobulin und 11S-Pflanzenprotein (-NH3+; COO-) und Polysacchariden (z.B. Pektin mit -COO- und ι-Carrageen mit -OSO3-) in Abhängigkeit vom pH-Wert.
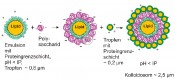
Abb.2a „Einschritt-Verfahren“, Emulsionsherstellung mit Gemisch aus Protein und ionischem Polysaccharid.
Abb.2b „Zweischritt-Verfahren“, Emulsionsbildung mit Protein, Zugabe ionischer Polysaccharide zur Emulsion.
Abb.3 Mit Molkenprotein stabilisierte multiple W/O/W-Emulsionen; A1, Öltropfenverteilung bei pH 5, Herstellung nach „Einschritt-Verfahren“, A2, Tropfenaggregatebildung bei pH 5 , Herstellung nach „Zweischritt-Verfahren“.
Einstellung der Emulsionseigenschaften, Beeinflussung der Tropfenaggregatebildung Bei der Herstellung von Öl-in-Wasser-Emulsionen (O/W) auf Basis biologischer Rohstoffe werden neben dem Fließverhalten bzw. der Konsistenzeigenschaft auch bestimmte Anforderungen an die Stabilität und Freisetzung bzw. Verfügbarkeit verschiedener Inhaltsstoffe (z.B. bioaktive, gesundheitsfördernde, geschmacks-, geruchs- und duftgebende) gestellt. Die derzeitige Herausforderung besteht darin, maßgeschneiderte Emulsionseigenschaften unter Einsatz biologischer Rohstoffe zu erzielen und auch die „Clean-Label“-Anforderungen erfüllen zu können. Ein derartig hoher Anspruch kann realisiert werden, wenn zur Emulsionsherstellung Naturstoffe (z.B. emulgierende Proteine, ionische Polysaccharide) eingesetzt werden, deren Eigenschaften konstant und deren Interaktionen beherrschbar sind. Weiterhin müssen die Einflüsse der Milieubedingungen (pH-Wert, Elektrolytgehalt, Anteil mehrwertiger Metallionen), der molekularen Stoffeigenschaften, des Ladungspotenzials sowie der Biopolymerverhältnisse bekannt sein. Wie in Abbildung 1 dargestellt, weisen die ionischen Biopolymere in wässriger Lösung abhängig vom pH-Wert ein unterschiedlich elektrisches Potenzial (mV) auf (ermittelt durch Zeta-Potenzialmessung bzw. Bestimmung der elektrophoretischen Mobilität im elektrischen Feld). Dieser Ladungszustand wird zusätzlich durch den Entfaltungszustand der Biopolymere (z.B. Denaturierungsgrad der Proteine) und die Elektrolytkonzentration bestimmt. Während in Lösungen mit Protein-Polysaccharid-Gemischen die Absenkung des pH-Wertes z.B. auf pH 3 infolge des entgegengesetzten Ladungszustandes zu Bildung unlöslicher oder löslicher Komplexe führt, bewirkt ein hoher negativer Ladungszustand (z.B. pH 7) eine elektrostatische Abstoßung der Polymerkolloide. Das ist insbesondere für die Stabilitätsverbesserung von Emulsionen von Bedeutung, wenn die Proteingrenzschichten an den Emulsionstropfen eine hohe negative Ladung aufweisen und die kontinuierliche Phase anionische Polysaccharide enthält. Hierdurch werden eine Tropfenaggregation (bzw. Agglomeratebildung) infolge repulsiver elektrischer Ladung (elektrostatische Stabilisierung) verhindert und somit die Emulsionsstabilität verbessert. Derartige Effekte können realisiert werden, wenn während der Emulsionsherstellung zugleich anionische Proteine und Polysaccharide anwesend sind (Einschritt-Verfahren, Abb. 2a) [2]. Erfolgt erst die Herstellung der Emulsion mit Proteinen als Emulgator und danach die Zugabe eines anionischen Polysaccharids, ist überwiegend eine Tropfenaggregatebildung zu beobachten, die zur Phasentrennung und zum Wasserabsatz führt (Zweischritt-Verfahren, Abb. 2b). Werden nach dem „Einschritt-Verfahren“ in Abwesenheit von Ca-Ionen die Proteine (z.B. Molkeprotein) gemeinsam mit Na-Alginat oder niederverestertem Pektin eingesetzt, kann die Emulsion nachträglich durch Zugabe von Ca-Salz in ein Emulsionsgel umgewandelt werden [3]. Eine weitere Möglichkeit der Fixierung der Emulsionsstruktur besteht in der zusätzlichen Ausbildung kovalenter Bindungen zwischen den Proteinmolekülen (z.B. Disulfidbindungen) mittels thermischer Behandlung. Über die Vermeidung der Tropfenaggregatebildung sind fließfähige Emulsionen nicht nur in der Phasenstabilität, sondern auch im Mundgefühl hinsichtlich cremig, sahnig, vollmundig oder auch für spezielle Anwendungseigenschaften einstellbar, wie sie für Lotions, Cremes oder Pasten erforderlich sind. Abbildung 3 zeigt Beispiele für Emulsionen (Wasser-in-Öl-in-Wasser, W1/O/W2), hergestellt nach dem Einschritt- oder Zweischritt-Verfahren. Beispiel A1 zeigt keine Tropfenaggregation („Einschritt-Verfahren“), die W1-Phase enthält unterschiedliche wasserlösliche Komponenten (Aromen, Vitamine, Wirkstoffe usw.). Diese Emulsion weist sehr gute Fließeigenschaften auf. Beispiel A2 zeigt Tropfenaggregate, die in konzentrierten Emulsionen je nach Kompaktheit der Aggregate die Fließgrenze erhöhen und zur Konsistenzgebung beitragen. Emulsionen mit Biopolymer-Multischichten Die Kenntnisse über pH-abhängige Ladungszustände der verschiedenen Biopolymere in wässrigen Lösungen und Emulsionen ermöglichen den Aufbau mehrschichtiger Grenzflächen an dispergierten Öltropfen. Hierüber kann die Stofffreisetzung eingeschlossener Komponenten für unterschiedliche Milieubedingungen eingestellt werden, so z.B. die Freisetzung beim Kauvorgang, bei pH-Änderung oder im mittleren oder unteren Verdauungstrakt. Sollen O/W-Emulsionen eine Ölphase mit öllöslichen Komponenten enthalten, die vor Oxidation geschützt und unter bestimmten Bedingungen freigesetzt werden, kann diese Eigenschaft gut in verdünnten Emulsionssystemen über einen Mehrschichtenaufbau (Protein-Polysaccharid-Grenzflächen) realisiert werden [4, 5]. Hierbei muss jedoch während der Beschichtung eine Tropfenaggregatebildung durch Vorschaltung eines Waschprozesses verhindert werden. Realisiert wird die Bildung von Mehrschichtengrenzflächen („layer-by-layer“-Technik) durch Einstellen eines bestimmten Ladungszustands an proteinhaltigen Ölgrenzflächen (z.B. pH < IEP) und Dispergieren derartiger Öltropfen in Lösungen, die entgegengesetzt geladene Polymere enthalten (z.B. Polysaccharide bei pH 4, siehe Abb. 4). Die Barrierewirkung (z.B. Oxidationsschutz, Stofffreisetzung, Verdaulichkeit) ist über die Anzahl der Schichten einstellbar und durch zusätzliche Vernetzung der Schichten (z.B. Vernetzung von Pektin mittels Laccase [6]) möglich. Die hier geschilderte Multischichtenbildung ist auch durch Kombination von Proteinen möglich, wenn diese unterschiedliche IEP aufweisen. So kann z.?B. bei pH 7 ein mit β-Lactoglobulin beschichteter Öltropfen (IEP = ~ 5, negativ geladen) mit Lactoferrin (IEP ~ 8, positiv geladen) beschichtet [7] werden.
Abb.4 Prinzip der Bildung von Protein-Polysaccharid-Multischichten an O/W-Grenzflächen (regulierte Biopolymeradsorption über pH-Einstellung und Waschprozess).
Abb.5 Bildung einer Öltropfen-Grenzschicht („Kolloidosom“) zur Erhöhung der Aggregationsstabilität und zum Schutz der inneren Lipidphase [8]. Emulsionen mit „Tropfenbeschichtung“ In ähnlicher Weise wie beim Aufbau von Multischichten ist auch die Bildung einer zusätzlichen Grenzschicht aus Öltropfen möglich („Kolloidosom“-Bildung). Dies erfolgt durch Vermischen unterschiedlich geladener Tropfen bei pH 4, wobei Emulsionen mit positiv geladenen kleineren Öltropfen (z.B. Ø 0,2µm, β-Lactoglobulin-Grenzschicht) mit negativ geladenen Öltropfen (z.B. Ø 0,6µm, β-Lactoglobulin-Pektin-Grenzschicht) vermischt werden (Abb. 5). Neben dem Einsatz von Protein-Polysaccharid-Lösungen zur Bildung der äußeren aggregationsstabilen Grenzschicht können auch Polysaccharid-Konjugate (der MAILLARD-Reaktion ähnliche Verbindungen zwischen Proteinen und Polysacchariden) als O/W-Emulgatoren in multiplen Emulsionen eingesetzt werden [9]. Diese erhöhen die Aggregationsstabilität der Emulsion im säurehaltigen Milieu und bilden eine zusätzliche Barriere für den Stoffschutz (z.B. verkapseltes Fischöl oder Carotinoide in der inneren O-Phase). Zusammenfassung Mittels „molekularer“ Emulsionstechnologie können Mikrostrukturen (Biopolymer-Grenzschichten an den Emulsionstropfen) gezielt aufgebaut werden, diese verleihen Emulsionen vielseitige Anwendungseigenschaften und eine unterschiedliche Stofffreisetzung. Über Interaktionen zwischen Proteinen und ionischen Polysacchariden ist die Tropfenaggregate- bzw. Netzwerkbildung in Emulsionen beeinflussbar und somit zur Erzeugung von Makrostrukturen, zur Viskositätseinstellung oder Texturgebung geeignet. Aus den Mikro- und Makrostrukturen resultierende Eigenschaften sind sowohl im Food- als auch im Kosmetik- und Pharmabereich nutzbar.
Literatur Foto: © Fotolia.com / sergojpg |
L&M 7 / 2013
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Der Autor:Weitere Artikel online lesenNewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |