|
Forscher
>
Prof. Dr. Hendrik Fuchs
>
Tödliche Eiweiße in der Tumortherapie
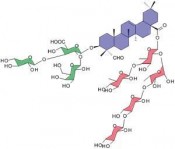
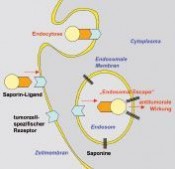
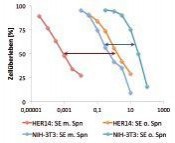
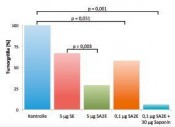
Tödliche Eiweiße in der TumortherapieZelluläre Zäune überwindenTumoren vollständig zu entfernen, ohne gesundes Gewebe zu schädigen, ist das Ziel jeder Krebstherapie. Zumeist gestaltet sich dies jedoch schwierig, weil die Begrenzung des Tumors nicht eindeutig zu bestimmen ist, der Tumor unzugänglich ist oder weil die Art des Tumors mit einer Streuung über den gesamten Körper einhergeht wie z. B. bei Leukämien. Selbst bei gut abgegrenzten und klar zu lokalisierenden Tumoren können sich einzelne Zellen lösen und an anderer Stelle neue Tumorherde, so genannte Metastasen, bilden. Neue eiweißbasierte Substanzen sollen helfen, Tumorzellen zielgerichtet zu erkennen und zu eliminieren. Tumorzellen finden Es gibt zwei besonders bedeutsame Herausforderungen bei der Entwicklung einer zielgerichteten Tumortherapie. Die erste ist die Frage, wie die einzelnen Tumorzellen im Körper ausfindig gemacht und als solche möglichst zweifelsfrei identifiziert werden können. Die zweite Herausforderung ist es, eine wirksame Substanz in die gefundene Tumorzelle einzubringen, um diese möglichst nach einem programmierten Ablauf reguliert zu töten oder zumindest effektiv an einer weiteren Vermehrung zu hindern. Ein anschaulicher Vergleich mag der Besuch in einem Zoo darstellen, in dem man ohne Lageplan und Schlüssel versucht, in das Robbengatter zu gelangen, um dort Fische zu verfüttern. Man kann unter Umständen stundenlang die Wege abschreiten, ohne erfolgreich zu sein, da die Gehege von außen mehr oder weniger gleich aussehen. Doch es gibt feine Unterschiede: Jedes Gehege besitzt Schilder, auf denen die darin lebenden Tiere beschrieben sind, sodass das Robbengatter identifiziert werden kann. Ähnlich präsentieren Tumorzellen an ihrer Oberfläche bestimmte Eiweiße (Rezeptoren), die sie von gesunden Zellen unterschieden. Allerdings sind diese Moleküle von Tumorart zu Tumorart und oft auch in unterschiedlichen Regionen eines Tumors verschieden und häufig kommen diese Moleküle, wenn auch in deutlich geringerer Anzahl, ebenso auf gesunden Zellen vor. Die modernen molekularbiologischen Techniken erlauben es inzwischen, natürliche Eiweißstoffe des Immunsystems, die Antikörper, künstlich herzustellen und dabei so zu verändern, dass sie gezielt die tumorzellspezifischen Oberflächenmoleküle erkennen [1]. Statt der Antikörper können auch andere Moleküle mit vergleichbaren Eigenschaften Verwendung finden; man spricht dann allgemein von tumorzellspezifischen Liganden. Tödliche Eiweiße Die Bindung eines Antikörpers an eine Tumorzelle reicht in der Regel nicht aus, um diese im Wachstum zu blockieren, auch wenn es einige erfolgreiche Therapieansätze dieser Art gibt [2]. Daraus entwickelte sich die Idee, diese Antikörper mit einem Giftstoff (Toxin) zu versehen. Besonders potente Toxine stammen aus den Bakterien Corynebacterium diphtheriae und Pseudomonas aeruginosa sowie aus bestimmten Pflanzen der Nelken- und Wolfsmilchgewächse. Diese Toxine sind wie auch die Antikörper Eiweiße (Proteine). Mithilfe der Molekularbiologie ist es daher möglich, einen Zusammenschluss aus Antikörper und Toxin herzustellen (Fusionsprotein), der nunmehr beide wichtigen Eigenschaften, d. h. Erkennung der Tumorzelle und toxische Wirkung, in sich vereinigt (Abb. 1). Mittlerweile sind etwa 50 solcher auch als zielgerichtete Toxine bezeichneten Fusionsproteine in verschiedenen Phasen der klinischen Testung [3]. Zelluläre Zäune überwinden Wenn wir noch einmal unseren Vergleich mit dem Zoo heranziehen, so haben wir jetzt zwar das Robbengatter gefunden und den Fisch zum Füttern fest bei uns, noch stehen wir aber vor einem schier unüberwindbaren Zaun. Bei den Zellen ist dieser Zaun die Zellmembran. Anders als bei einem Zaun ist diese Membran jedoch sehr beweglich und kann auch Einstülpungen ausbilden, die sich abschnüren (Abb. 2). Dieser Vorgang, die Endocytose, führt zwar zur Aufnahme des zielgerichteten Toxins in die Zelle, der Wirkort der Toxine liegt jedoch in der Zellflüssigkeit, dem Cytoplasma, und nicht im Lumen der abgeschnürten Vesikel, den Endosomen. Das Toxin muss also entweder direkt die Zellmembran oder die endosomale Membran durchqueren. Aufgrund der physikalischen Eigenschaften von Proteinen und Membranen kommt eine solche Durchquerung praktisch nicht vor, sodass die Wirkung der zielgerichteten Toxine größtenteils verpufft und ihr Potenzial bei Weitem nicht ausgenutzt wird. Seifen nicht nur zum Waschen In unserer Arbeitsgruppe haben wir uns daher zum Ziel gesetzt, die Durchquerung der zellulären Membranen für die zielgerichteten Toxine substanziell zu verbessern. Die Moleküle der Membranen besitzen zahlreiche Fettsäuren. Daher lassen sich Membranen – ähnlich wie Fett beim Waschen der Hände – mit seifenartigen Substanzen auflösen. Nun gibt es natürlich keinen Sinn, mithilfe der Seifen alle Membranen mit Löchern zu versehen, da der Effekt ähnlich wäre wie im Zoo, wenn alle Zäune durchlässig wären: Es würde unkontrolliertes Chaos herrschen. Im Rahmen unserer Forschungen ist es uns jedoch gelungen aus zwei Pflanzen, dem Seifenkraut (Saponaria officinalis) und dem Schleierkraut (Gypsophila paniculata), seifenartige Substanzen (Saponine) zu isolieren und zu identifizieren (Abb. 1), die in der Lage sind, sich in endosomale Membranen einzulagern und dabei den Durchtritt („Endosomal Escape“) von solchen Toxinen, die aus Nelkengewächsen stammen, zu ermöglichen. Zwar erfolgt die Einlagerung dieser Saponine in die Endosomen aller Zellen, also auch in gesunde, da jedoch die Toxine aufgrund der Kopplung an den tumorzellspezifischen Liganden vorwiegend nur in die Endosomen derjenigen Zellen gelangen, auf deren Oberfläche sich die dazu passenden Rezeptoren befinden, bleibt die Spezifität erhalten. Synergistische Effekte Die Wirkung einer kombinierten Therapie aus Saponinen und zielgerichteten Toxinen wurde von uns zunächst im Zellkulturmodell getestet. Das zielgerichtete Toxin besteht aus Saporin, einem pflanzlichen, die zelluläre Proteinsynthese inhibierenden Protein, und dem Liganden für einen Wachstumsfaktorrezeptor, der bei einigen häufigen Tumorarten stark vermehrt auf der zellulären Oberfläche erscheint. Dieses Fusionsprotein (SE genannt) wurde in Gegenwart und Abwesenheit von Saponinen sowohl an Zellen, die den Zielrezeptor tragen, als auch zur Kontrolle der Spezifität an zielrezeptorfreien Zellen getestet (Abb. 3 und 4). Das Ergebnis zeigt, dass es durch Vorbehandlung mit den von uns identifizierten Saponinen zu einer drastischen Erhöhung der Wirkung des zielgerichteten Toxins kommt, die mehr als millionenfach sein kann. Dieser Effekt ist daran erkennbar, dass bei einer enorm geringeren Konzentration des zielgerichteten Toxins die gleiche Anzahl an Zellen getötet wird. Auch bei den Kontrollzellen kommt es zu einer Erhöhung der Toxizität, jedoch ist der Effekt hier wesentlich geringer, sodass sich die therapeutische Breite, also die Konzentration, bei der eine Wirkung ohne wesentliche Nebenwirkung auftritt, erheblich vergrößert hat (Breite des Pfeils in Abb. 3). Damit können die zielgerichteten Toxine nunmehr sehr effektiv eingesetzt werden. Wichtig zu bemerken ist, dass der beobachtete Verstärkungseffekt nicht einfach die Addition zweier Effekte ist, sondern dass es sich um eine (bislang im Detail noch nicht aufgeklärte) gegenseitig verstärkende (synergistische) Wechselwirkung handelt, da beide Substanzen überhaupt keinen oder nur einen geringfügigen Effekt zeigen wenn sie jeweils allein in den Konzentrationen verabreicht werden, die für die Kombina tion angewendet werden. Tumortherapie im Mausmodell Im Anschluss an die Zellkulturexperimente haben wir die Therapie in einem Brustdrüsen tumormodell an der Maus getestet. Die Mäuse wurden bei jeder Behandlung zunächst mit Saponinen vorbehandelt, bevor eine Stunde später die zielgerichteten Toxine (SE und die Variante SA2E) verabreicht wurden. Als Vergleich diente die Behandlung ohne vorherige Gabe der Saponine. Unsere Experimente zeigten, dass die Saponine nach einer Stunde bereits größtenteils über den Urin ausgeschieden wurden [4]. Ein kleiner Teil hat sich jedoch wie erhofft in den endosomalen Membranen eingelagert. In der Kombinationstherapie wurden nur wenige geringfügige Nebenwirkungen beobachtet, die alle reversibel waren. Obwohl vom zielgerichteten Toxin nur ein Fünfzigstel der Menge eingesetzt wurde, die ohne Gabe von Saponinen erforderlich ist, um einen durchschnittlichen Rückgang von 71 % zu erzielen [5], wurde in Kombination mit Saponinen ein Rückgang der Tumoren von 94 % erzielt (Abb. 5) [6]. Wurde die in der Kombination verwendete Konzentration des zielgerichteten Toxins ohne Saponin eingesetzt, wurde lediglich ein Rückgang der Tumorgröße um 42 % beobachtet. Die Abbildung zeigt auch, dass die Variante SA2E wirksamer ist als SE. Der durch bestimmte Saponine vermittelte immense Verstärkungseffekt in der Wirksamkeit erlaubt den Einsatz sehr geringer Dosen. Dies verringert nicht nur die Immunreaktion des Organismus gegen die körperfremden Proteine, sondern hat darüber hinaus auch eine wirtschaftliche Bedeutung für die Produktion solcher Wirkstoffe, da die Herstellung von proteinbasierten Medikamenten sehr teuer ist. Ausblick Die Kombinationstherapie aus zielgerichteten Toxinen und pflanzlichen Saponinen stellt einen neuartigen und viel versprechenden Ansatz in der Tumortherapie dar. Die für klinische Studien erforderliche Etablierung einer qualitätsgesicherten Produktion der einzelnen Komponenten erfordert jedoch noch mehrjährige Forschungstätigkeit.
Literatur Foto: © Prof. Dr. Hendrik Fuchs |
L&M 2 / 2012
Das komplette Heft zum kostenlosen Download finden Sie hier: zum Download Der Autor:NewsSchnell und einfach die passende Trennsäule findenMit dem HPLC-Säulenkonfigurator unter www.analytics-shop.com können Sie stets die passende Säule für jedes Trennproblem finden. Dank innovativer Filtermöglichkeiten können Sie in Sekundenschnelle nach gewünschtem Durchmesser, Länge, Porengröße, Säulenbezeichnung u.v.m. selektieren. So erhalten Sie aus über 70.000 verschiedenen HPLC-Säulen das passende Ergebnis für Ihre Anwendung und können zwischen allen gängigen Herstellern wie Agilent, Waters, ThermoScientific, Merck, Sigma-Aldrich, Chiral, Macherey-Nagel u.v.a. wählen. Ergänzend stehen Ihnen die HPLC-Experten von Altmann Analytik beratend zur Seite – testen Sie jetzt den kostenlosen HPLC-Säulenkonfigurator!© Text und Bild: Altmann Analytik ZEISS stellt neue Stereomikroskope vorAufnahme, Dokumentation und Teilen von Ergebnissen mit ZEISS Stemi 305 und ZEISS Stemi 508ZEISS stellt zwei neue kompakte Greenough-Stereomikroskope für Ausbildung, Laborroutine und industrielle Inspektion vor: ZEISS Stemi 305 und ZEISS Stemi 508. Anwender sehen ihre Proben farbig, dreidimensional, kontrastreich sowie frei von Verzerrungen oder Farbsäumen. © Text und Bild: Carl Zeiss Microscopy GmbH |